TUMEURS stromales gastro-intestinales (GIST): La FDA approuve Glivec® sur 3 ans
La Food and Drug Administration (FDA) vient d’approuver Glivec ® (imatinib) de Novartis en traitement de 3 ans, après chirurgie, pour les patients atteints de tumeurs stromales gastro-intestinales (GIST). Glivec vient en effet de démontrer dans un essai de phase III son efficacité à réduire de 54% le risque de récidive et de décès chez ces patients, par traitement de 3 ans vs 1 an.
Cette approbation qui s'appuie sur l'historique de plus de 10 ans d'utilisation de Glivec pour le traitement des GIST a fait l'objet d'une procédure d'évaluation prioritaire de la FDA. Une mise à jour de la notice de Glivec ® (imatinib) va donc être effectuée avec la recommandation d'un traitement de 36 mois après la chirurgie, pour les patients adultes atteints tumeurs stromales gastro-intestinales (GIST) KIT (CD117) positives. Ces 36 mois de traitement par Glivec ont entraîné une réduction de 54% du risque de récidive et de 55% du risque de décès par rapport à un an de traitement, selon les résultats de l'essai de phase III qui portait sur 387 patients. «Avec le bénéfice de survie significatif résultant de trois ans de traitement adjuvant, les patients atteints de GIST ont maintenant une option plus efficace pour gérer leur maladie », résume Hervé Hoppenot, Président de Novartis Oncologie.
Les tumeurs stromales gastro-intestinales sont rares. Leur cause principale est une forme anormale de la protéine KIT qui induit une croissance incontrôlée des cellules qui deviennent cancéreuses. Les patients atteints de GIST sont à risque élevé de récidive après résection complète des GIST primaires. Depuis août 2011, le réseau américain National Comprehensive Cancer Network (NCCN) recommande déjà au moins trois ans de traitement adjuvant par Glivec pour les patients à risque élevé de récidive atteints de GIST.
Glivec ® (imatinib) est aujourd'hui approuvé dans plus de 110 pays pour le traitement de toutes les phases des GIST KIT (CD117) positives qui ne peut être enlevées chirurgicalement et / ou ont métastasé et pour le traitement des patients adultes après ablation chirurgicale complète de la tumeur.
Sources: FDA « Imatinib Mesylate Tablets », Novartis “FDA approves Novartis drug Glivec® label recommending extending treatment to three years for certain GIST patients after surgery »
Accéder à d'autres actualités sur Glivec
Devenez membre PREMIUM
Accèdez sans limite aux 15 000 actualités du site
et recevez gratuitement chaque semaine,
la Newsletter Santé log avec les actus Santé à ne pas manquer !

Je suis déjà membre PREMIUM
Autres actualités sur le même thème
CANCER du SEIN: Cellules tumorales circulant dans le sang, signe de mauvais pronostic
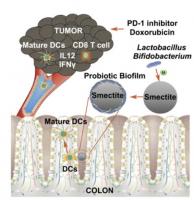
Actualité publiée il y a 12 années 10 moisIMMUNOTHÉRAPIE du cancer : Des microsphères de smectite pour la booster
Actualité publiée il y a 4 années 1 moisCANCER du SEIN: Découverte d'un nouveau type de mutation
Actualité publiée il y a 12 années 11 moisCes chercheurs de la Mayo Clinic ont découvert une nouvelle classe de mutation moléculaire pour diverses formes de cancer du sein, une découverte qui pourrait...VACCINS: Les labos interdits de publicité auprès du grand public
Actualité publiée il y a 12 années 8 mois